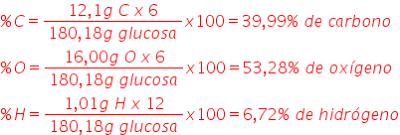Compuestos,
enlaces químicos y masas moleculares
Compuestos
Un
compuesto es una sustancia pura que aún se puede separar en otras más simples
por métodos químicos.
Por
ejemplo, el agua es una sustancia pura, pero si la sometemos a electrolisis (proceso químico) la podemos separar en sus elementos constituyentes: el oxígeno
y el hidrógeno.
En
un compuesto hay átomos de diferentes elementos unidos mediante fuerzas que
denominamos enlaces químicos.
1.1
Fórmula molecular y empírica
·
Formula molecular. La fórmula molecular es la fórmula química
que indica el número y tipo de átomos distintos presentes en la molécula. La
fórmula molecular es la cantidad real de átomos que conforman una molécula.
·
Fórmula empírica. La fórmula empírica nos muestra la proporción
entre los átomos de un compuesto químico. A veces puede coincidir con la
fórmula molecular del compuesto.
1.2
Compuestos binarios
Son
los formados por dos elementos diferentes. Los más importantes son:
·
Óxidos. Son combinaciones del oxígeno con otro elemento,
metálico o no metálico.
·
Hidruros. Son
combinaciones entre el hidrógeno y otro elemento, metálico o no metálico.
·
Sales binarias. Son combinaciones entre un metal y un no
metal.
1.3
Compuestos ternarios
Son
los formados por tres elementos diferentes. Los más importantes son:
·
Hidróxidos. Son combinaciones de un metal con grupos
hidroxilo (OH-).
·
Ácidos oxoácidos. Son combinaciones entre un no metal con
oxígeno e hidrógeno.
·
Sales oxisales. Son combinaciones entre un metal, un no metal y
oxígeno.
2. Enlace Químico
Los
responsables de la formación de un enlace químico son los electrones.
Los
enlaces químicos se forman para que los átomos que intervienen en el enlace
completen su capa de valencia.
Según
como tengan lugar la uniones de los átomos podemos distinguir los siguientes
tipos de enlace:
·
Enlace iónico: se produce cuando existe un intercambio de
electrones entre los átomos de un metal y un no metal. Al intercambiarse
electrones se forman iones positivos y negativos que se atraen debido a
sus cargas opuestas.
·
Enlace covalente: se produce cuando los átomos enlazantes
comparten electrones para completar su última capa.
·
Enlace metálico: ocurre solamente entre átomos de un mismo
elemento metálico.
2.1
La regla de octeto
La
regla del octeto, enunciada en 1916 por Gilbert Newton Lewis, dice que la
tendencia de los iones de los elementos del sistema periódico es completar sus
últimos niveles de energía con una cantidad de 8 iones que tienen carga
negativa, es decir, electrones, de tal forma que adquiere una configuración muy
estable.
Esta
configuración es semejante a la de un gas noble, los elementos ubicados al
extremo derecho de la tabla periódica. Los gases nobles son elementos
electroquímicamente estables ya que cumplen con la estructura de Lewis,
son inertes, es decir, que es muy difícil que reaccionen con algún otro
elemento.
Es
importante saber que la regla del octeto es una regla práctica aproximada que
presenta numerosas excepciones, pero que sirve para predecir el comportamiento
de muchas sustancias.
3. Masas Moleculares
La
masa molecular es la masa que tiene una molécula.
Para
determinar la masa molecular sumaremos las masas de todos los átomos que
constituyen la molécula.
3.1
Mol
Un
mol es la cantidad de materia que contiene 6,02x1023 (número de Avogadro) partículas
elementales, ya sean átomos, moléculas, iones, partículas subatómicas, etc...
Por
eso, cuando un químico utiliza el término mol, debe dejar claro si es:
1
mol de átomos
1
mol de moléculas
1
mol de iones
1
mol de cualquier partícula
3.2
Masa molar
Se
llama masa molar de una sustancia a la masa de un mol de dicha sustancia y se
expresa gramos/mol ( g/mol);
por ejemplo:
Masa
molar del Fe = 55,8 g/mol
Masa
molar del H2O = 18 g/mol
Podríamos
decir que la masa molar es lo mismo que la masa molecular, pero en vez de estar
en unidad de masa atómica (u) está en gramos/mol.
La
masa molar de un compuesto se calcula fácilmente conociendo las masas molares
de los elementos que lo forman y la fórmula del compuesto.
3.3
Composición centesimal
Es
la proporción entre la masa de un elemento y la masa total del compuesto
químico, expresada en tanto por ciento.
----0----
Ejemplo:
Calcular la composición centesimal de la glucosa,
un monosacárido cuya fórmula molecular es C6H12O6
Masas atómicas (g/mol):
Ma(H) = 1,01
Ma(C) = 12,01
Ma(O) = 16,00
Solución:
Masa molar (glucosa) = 12,01 x 6 + 1,01 x 12 + 16,00 x 6 = 180, 18 g/mol